في علاج السرطان، لا يبدأ التحدي الحقيقي من اختيار الدواء؛ بل من سؤال أكثر حساسية وعمقاً: هل سينجح هذا العلاج مع هذا المريض تحديداً؟
هذا السؤال، الذي لازم الممارسة الطبية لعقود، ظل في كثير من الأحيان بلا إجابة حاسمة؛ تُقدَّر فيه الاحتمالات ولا تُحسم فيه النتائج. وبين قرارٍ يُتخذ وأملٍ يُعلّق، قد يجد المريض نفسه أمام علاج معقد ومكلف دون أن يكون هو الخيار الأنسب له.
مؤتمر الجمعية الأميركية لأبحاث السرطان
غير أن ما كُشف عنه حديثاً في مؤتمر الجمعية الأميركية لأبحاث السرطان (AACR 2026) المنعقد في شيكاغو، إلينوي، بين 25 و30 أبريل (نيسان) 2026، يشير إلى تحول نوعي في هذا المسار؛ إذ لم تعد الإجابة تُستنبط من الفحوصات الجزيئية وحدها، بل قد تكون كامنة في مكان أبسط بكثير... وأقرب إلى الممارسة اليومية: الشرائح النسيجية المأخوذة من خزعات الورم.
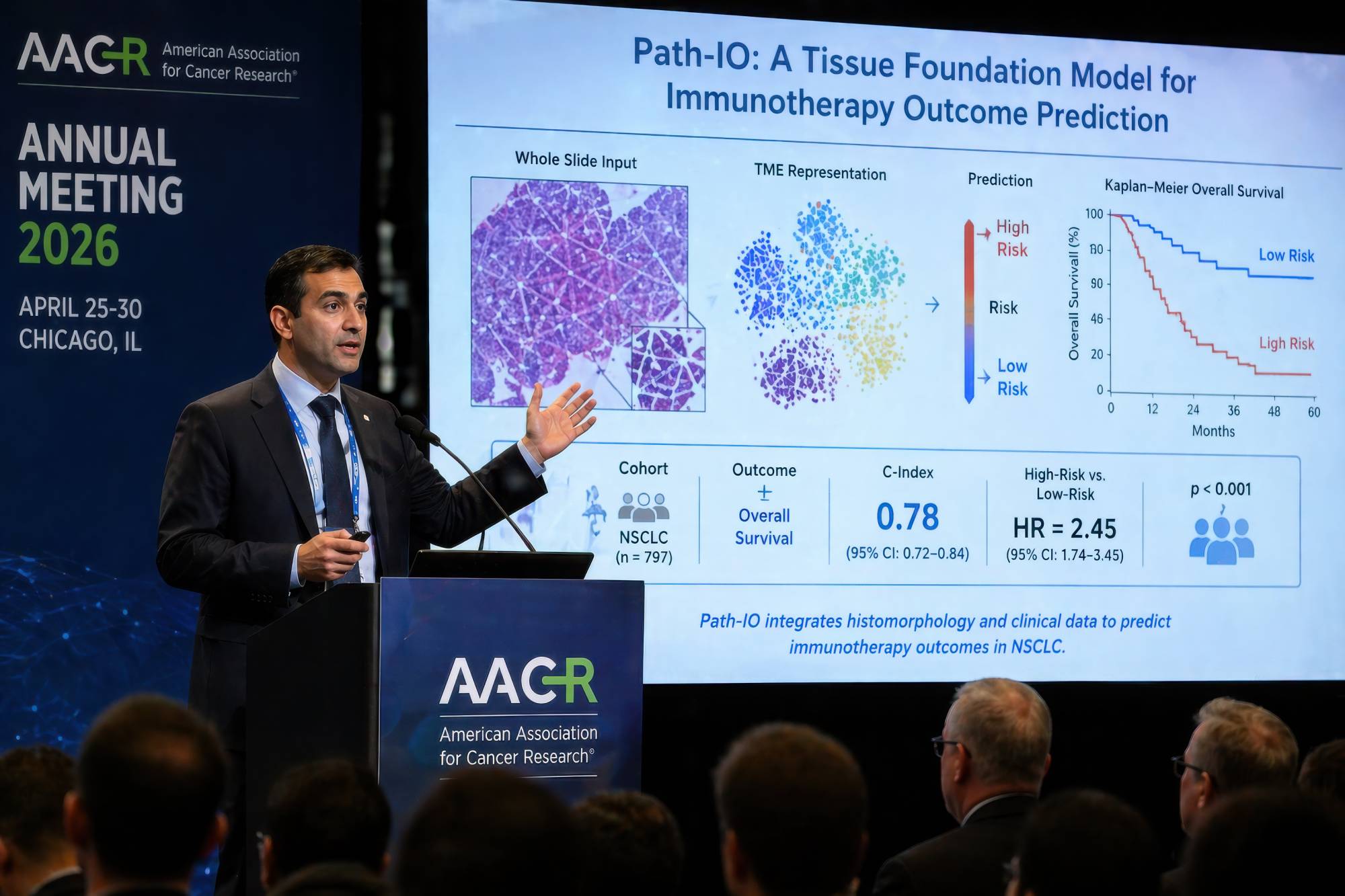
وفي هذا السياق، وخلال إحدى الجلسات العلمية الافتتاحية للمؤتمر، قدّم الباحث فيصل محمود (Faisal Mahmood) من كلية الطب بجامعة هارفارد، عرضاً لافتاً لنموذج متقدم من الذكاء الاصطناعي يعيد تعريف دور هذه الشرائح؛ لا بوصفها أداة للتشخيص فحسب، بل بوصفها مصدراً قادراً على الإسهام المباشر في توجيه القرار العلاجي.
حين تصبح الخزعة لغةً للتنبؤ
يُعدّ العلاج المناعي أحد أبرز إنجازات الطب الحديث في مواجهة السرطان، خصوصاً في أمراض مثل سرطان الرئة ذي الخلايا غير الصغيرة. ومع ذلك، يخفي هذا التقدم وراءه تحدياً معقّداً: إذ لا يستفيد منه كل المرضى منه بالقدر ذاته.
وفي الممارسة الحالية، يعتمد الأطباء على مؤشرات حيوية مثل بروتين «PD-L1» لتقدير احتمالية الاستجابة، لكنها تظل مؤشرات محدودة لا تكفي لاتخاذ قرار حاسم. وهكذا، قد يخضع بعض المرضى لعلاجات مرهقة ومكلفة، دون أن تكون هي الخيار الأمثل لهم.
ذكاء اصطناعي لتحليل الشرائح النسيجية
هنا يظهر دور النموذج الجديد، المعروف باسم «Path-IO»، وهو نظام ذكاء اصطناعي متقدم لتحليل الشرائح النسيجية في علم الأمراض الرقمي. هذا النموذج لا يقرأ الخلايا السرطانية بوصفها وحدات منفصلة؛ بل يتعامل مع خزعة الورم بوصفها بيئة حيوية متكاملة، ويغوص في تفاصيل ما يُعرف بـ«البيئة المجهرية للورم» - ذلك العالم المعقد من التفاعلات بين الخلايا السرطانية والخلايا المناعية داخل النسيج.
ومن خلال تقنيات التعلم العميق، يستطيع «Path-IO» التقاط الأنماط والعلاقات الخفية داخل هذه البيئة، واستخلاص إشارات دقيقة ترتبط بقدرة الجهاز المناعي على الاستجابة للعلاج، ليحوّل الخزعة من صورة تشخيصية صامتة إلى نصّ بيولوجي يمكن قراءته؛ بل واستشراف ما قد يحدث من خلاله.
حين تقلّ مساحة التخمين
في الدراسة التي شملت 797 مريضاً بسرطان الرئة، تمكّن النموذج من التمييز بوضوح بين المرضى الذين يُرجّح أن يستفيدوا من العلاج المناعي، وآخرين ترتفع لديهم أخطار تدهور المرض أو الوفاة.
ولا تعني هذه القدرة مجرد تحسين في الدقة التشخيصية؛ بل تعكس تحولاً أعمق: تقليص مساحة التخمين في الطب. فبدلاً من اتخاذ القرار استناداً إلى مؤشرات عامة، يصبح بالإمكان توجيه العلاج وفق قراءة دقيقة لبيولوجيا الورم نفسه.
لكن هذا التحول لا يعيد صياغة القرار فحسب؛ بل يمسّ جوهر الممارسة الطبية. فقد قام الطب طويلاً على مبدأ «التجربة ثم التقييم»، حيث يُختبر العلاج في جسد المريض قبل أن يُحكم عليه. أما اليوم، ومع دخول الذكاء الاصطناعي إلى قلب القرار، فنحن أمام مرحلة جديدة يصبح فيها التنبؤ سابقاً للتجربة، والمعرفة متقدمة على الفعل. وهنا لا يفقد الطبيب دوره، بل يتبدل موقعه؛ من مجرّد من ينتقي بين خيارات متاحة، إلى من يقرأ خريطة الاحتمالات قبل أن تتحول إلى واقع. وفي هذا التوازن الدقيق، لا يكون الذكاء الاصطناعي بديلاً عن القرار الطبي؛ بل مرآة أعمق له، تكشف ما كان خفياً، وتضع أمام الطبيب مسؤولية جديدة: أن يقرر... وهو يعرف أكثر مما كان يعرف من قبل.

من المختبر إلى سرير المريض
تكمن قوة هذا النموذج في بساطته الظاهرية؛ فهو لا يعتمد على تقنيات نادرة أو بيانات يصعب الحصول عليها، بل على الشرائح النسيجية التي تُستخدم يومياً في معظم المستشفيات حول العالم. وهذا يعني أن إدخاله إلى الممارسة السريرية لا يتطلب تغييرات جذرية في البنية التحتية، بقدر ما يستدعي إعادة قراءة لما هو متوفر أصلاً، لكن بعين مختلفة.
وفي العالم العربي، حيث يتزايد الاعتماد على العلاج المناعي ضمن استراتيجيات علاج السرطان، تبرز هذه النماذج فرصة حقيقية لإعادة توجيه القرار العلاجي، وتحسين كفاءة استخدام الموارد، وتقليل التكاليف الناتجة عن العلاجات غير الفعالة، وتعزيز تطبيقات الطب الدقيق - خصوصاً في ظل التحولات الصحية الكبرى التي تشهدها المنطقة، وفي مقدمتها رؤية المملكة العربية السعودية 2030.
طبّ لا يكتفي بالتشخيص
يمثل هذا النموذج جزءاً من اتجاه عالمي متسارع لإعادة تعريف دور الذكاء الاصطناعي في علم الأورام؛ فبعد أن ظل لسنوات أداة تدعم التشخيص وتُحسّن دقته، بدأ اليوم يتحرك نحو أفق أكثر تأثيراً: التنبؤ بمسار المرض، والمساهمة في توجيه القرار العلاجي. وهنا لا يعود الذكاء الاصطناعي مجرد أداة ترى ما هو موجود؛ بل صار نظاماً يحاول قراءة ما قد يحدث... قبل أن يحدث.
الخلاصة: متى نعرف... قبل أن نجرّب؟
ما يقدمه هذا النموذج لا يضيف اختباراً جديداً إلى قائمة الفحوصات؛ بل يغيّر طريقة قراءة ما هو موجود أصلاً. وهذا هو التحول الحقيقي في الطب الحديث: أن تصبح البيانات نفسها أكثر قدرة على الكلام دون أن تتغير، وأن تتحول الإشارات الصامتة داخل الأنسجة إلى دلائل يمكن فهمها؛ بل والاستناد إليها في اتخاذ القرار.
لكن هذا التحول لا يطرح سؤالاً تقنياً فحسب؛ بل يفتح باباً أعمق في فلسفة الطب. فحين يصبح بالإمكان التنبؤ بما قد ينجح قبل أن يُجرّب، تتغيّر طبيعة العلاقة بين الطبيب والعلاج، وبين المعرفة والفعل.
لم يعد السؤال: أي علاج نختار؟ ولا حتى: هل هذا هو الخيار الأفضل؟
بل أصبح السؤال الأعمق: هل نملك الشجاعة لنعرف... قبل أن نجرّب؟